澳門大學健康科學學院講座教授鄧初夏領導的研究團隊在癌細胞抗藥性機制研究方面取得突破性進展。研究指出,蛋白酶體參與調控由抗癌藥物誘導的ROS-BNIP3介導線粒體自噬過程,進而影響癌細胞的存活與抗藥性。該成果為克服癌症抗藥性提供新線索,並已發表於國際權威期刊《Drug Resistance Updates》。
腫瘤細胞的多重抗藥性與蛋白酶體活性增強和線粒體功能下降密切相關。蛋白酶體的活性有助於清除受損蛋白質,而線粒體功能降低則可能導致細胞進入靜止狀態。然而,蛋白質損傷、線粒體功能和蛋白酶體活性之間的機制聯繫仍未明確。澳大研究團隊利用螢光藥物、可誘導線粒體蛋白模型和質譜技術,探索相關因素在腫瘤多重抗藥性中的潛在關聯。
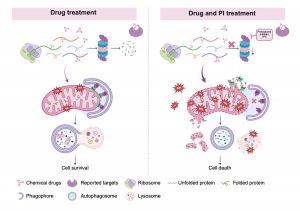
研究主要發現包括:一、化學藥物與新合成的線粒體蛋白質結合,並共同輸入線粒體;二、輸入線粒體的受損蛋白質會觸發線粒體—溶酶體介導的鏈式反應,包括整合壓力反應(ISR)和線粒體非折疊蛋白反應(UPRmt),隨後導致溶酶體生物合成增加及ROS-BNIP3介導的線粒體自噬;三、蛋白酶體透過監測蛋白質穩態、抑制線粒體蛋白質輸入和促進正常、藥物處理條件下的線粒體自噬,使癌細胞能對抗藥物處理而存活;四、蛋白酶體抑制劑硼替佐米(BTZ)可引發線粒體過度輸入受損蛋白質,造成線粒體膜損傷,嚴重的線粒體ROS產生和洩漏、溶酶體膜通透性增加,使線粒體自噬無法產生;五、BTZ+藥物聯合治療可透過抑制線粒體自噬而誘導一種新型的細胞死亡,從而克服腫瘤抗藥性。
該研究通訊作者為鄧初夏及澳大健康科學學院客席副教授徐曉玲,第一作者及共同第一作者分別為該學院博士生李玲、博士後馮楊洋。其他團隊成員包括該學院研究助理教授邵方元、孫恆,博士生唐東洋、林詩琪、褚祥鵬、喬雲峰、李杭杭,博士後周靖波、雷海鵬。該研究獲國家自然科學基金(檔案編號:82030094)、澳門特別行政區科學技術發展基金(檔案編號:0004/2021/AKP、0007/2021/AKP、0129/2024/RIA2、0054/2023/RIA1、0065/2021/A、0193/2024/AGJ和0009/2022/AKP)和澳大(檔案編號:CPG2025-00035-FHS、MYRG2022-00175-FHS、MYRG-GRG2023-00029-FHS-UMDF和MYRG-GRG2024-00073-FHS)資助。全文可瀏覽:https://www.sciencedirect.com/science/article/pii/S1368764625000974。
| 新聞來源:健康科學學院 | |
| 媒體聯繫: | |
| 澳門大學傳訊部 | |
| 李巧雲 | 電話:(853) 88228004 |
| 梁曉珊 | 電話:(853) 88228009 |
| 電郵: | prs.media@um.edu.mo |